コンテンツ

導入
水素が宇宙で最も豊富な元素であることをご存知ですか?文字 H で表される水素は、今日の世界で実用化されている多くの分子や化合物に含まれています。例えば、水素は生命の源である水を形成します。ただし、この元素はアンモニアなどの化学物質も生成し、洗浄製品によく含まれます。全体として、水素は地球上の生命の創造と維持にとって非常に重要な元素です。水素のモル質量を調べ、それが周期表上の他の元素とどのように比較されるかを確認します。
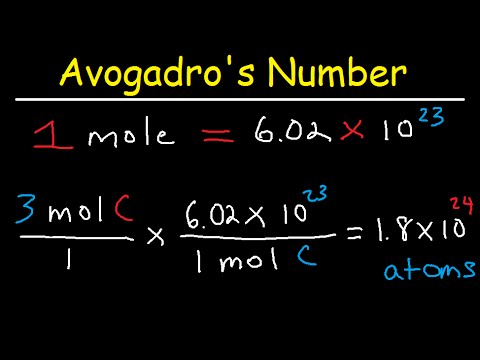
水素とは何ですか?
水素は周期表に記載されている最も単純な元素ですが、生命を維持する上で最も重要な元素の 1 つです。さらに、この元素には色や味はなく、気体の形をしています。水素の説明は全体的に印象的ではないように思えるかもしれませんが、その性質と用途は発展を続けており、医学、科学研究、化学において大きな可能性を秘めています。
水素原子は、負の電荷をもつ電子に囲まれた中心核で構成されています。さらに、原子核には正の電荷を持つ陽子が 1 つ含まれています。周期表の他の多くの元素は原子内に複数の電子を持っていますが、水素には取り囲む電子が 1 つだけ含まれています。
水素ガスはいくつかの水素分子で構成されており、化学式 H
2
を持つ 2 つの水素原子で構成されています。水素は、酸素と結合して水を形成し、式 H
2
O で表されるため、特に重要です。さらに、水素は宇宙全体で最も豊富な元素です。水素ほど頻繁に自然に発生する元素は他にありません。地球上では、この元素は海や
などの水源、氷、氷河、空気中に存在します。

モル質量とは何ですか?またその計算方法は何ですか?
元素のモル質量を理解するには、
モル
の概念を確認する必要があります。 「モル」という用語は、元素または化合物の質量内の原子や分子などの小さな実体の数を表します。モルを計算するために、科学者や化学者は
アボガドロ数
と呼ばれる値を使用します。アマデオ アボガドロは、1 モル内の原子または分子の数を表すアボガドロ数を最初に理論化しました。数値は 6.022 x 10
23
です。
科学者は、物質の質量 (グラム単位) を物質のモル数で割ることによってモル質量を計算します。周期表では、単一元素のモル質量がその命名法の下にリストされています。これらの値は、特定の要素の命名法の下にあります。ただし、これらの値は、モル質量ではなく、元素の原子質量と呼ばれることがよくあります。単一元素のモル質量を報告するには、原子質量値を参照し、単位 g/mol を追加します。
分子のモル質量
ただし、化合物または分子の場合、モル質量を求めるにはさらなる手順が必要です。たとえば、H
2
O または水を考えてみましょう。水素 (H) の原子量は 1.00784、酸素 (O) の原子量は 15.9994 です。水の分子の中には、1 つの酸素原子と並んで 2 つの水素原子が存在します。したがって、モル質量方程式は、化合物の特定の元素の原子数を考慮する必要があります。
したがって、H
2
O 中の水素原子のモル質量の計算は、方程式 2 x 1.00784 によって示されます。 H
2
O 中の酸素原子のモル質量の計算は、方程式 1 x 15.9994 で示されます。そこから、両方の方程式の積の合計により、H
2
O のモル質量が得られます。したがって、モル質量方程式の概要は次のとおりです。
(2 x 1.00784) + (1 x 15.9994) = 18.01508 g/mol
したがって、水のモル質量は 18 という値に四捨五入されます。
水素のモル質量は何ですか?
水素 (H) は単一元素であり、そのモル質量は簡単に見つけることができます。周期表には、文字 H の下に水素のモル質量が記載されています。ただし、元素水素は通常、水素ガスまたは水中に存在します。水のモル質量は上にリストされていますが、水素ガスのモル質量は何ですか?水素ガスの化学式は H
2
であり、水素ガスが 2 つの水素原子で構成されていることを意味します。したがって、水素ガスのモル質量を求める式は次のとおりです。
2 x 1.00784 = 2.016 g/mol

水素のモル質量と他の元素: 比較
| 要素 | 化学式 | モル質量 |
|---|---|---|
| 水素 | H | 1.00784 g/mol |
| ナトリウム | ナ | 22.98977 g/mol |
| 炭素 | C | 12.011 g/mol |
| 窒素 | N | 14.007 g/mol |
| 酸素 | ○ | 15.9994 g/mol |
| 塩素 | Cl | 35.45 g/mol |
| 亜鉛 | 亜鉛 | 65.4g/mol |
| ヨウ素 | 私 | 126.9045 g/mol |

水素分子と化合物のモル質量: 比較
| 分子・化合物 | 化学式 | モル質量 |
|---|---|---|
| 水素ガス | H2 | 2.016 g/mol |
| 水 | H2O | 18.01508 g/mol |
| クロロホルム | CHCl3 | 119.38 g/mol |
| アンモニア | NH3 | 17.031 g/mol |
| フッ化水素酸 | HF | 20.0063 g/mol |
| エタノール | C2H6O _ | 46.08 g/mol |

なぜ水素が重要なのでしょうか?
水素が生命の維持に不可欠である理由は数多くあります。まず、この元素は
太陽へ
の電力供給に役立ちます。太陽内での化学反応により水素の性質が変化し、ヘリウムに変わります。さらに、水分子を形成するには水素原子が必要です。水は通常、科学、文学、芸術などにおいて、すべての生命の源であると考えられています。したがって、水の存在とともに地球に運ばれる
太陽の
熱と光が、ここでの生命の繁栄を可能にしています。これらの自然要素がなければ生命は存在しません。このように、私たちはこの美しい世界に住んでいる水素に部分的に感謝する必要があります。
水素には一般的な用途もあり、多くの人が知らず知らずのうちに水素に触れています。たとえば、水素はさまざまな化学製品や肥料に含まれています。
アンモニア
は水素を含む一般的な化合物で、窓用洗剤、トイレ用洗剤、家具磨き剤などの製品に含まれています。さらに、メチル アルコールの生成には水素が必要で、メチル アルコールは塗料剥離剤、塗料、インクなどに含まれています。
さらに、溶接などの一部の作業には水素が必要です。溶接工は酸水素トーチを使用してさまざまな金属を溶かします。トーチに電力を供給するには、酸素と水素という元素の間で化学反応が起こります。したがって、金属を溶かすのに役立つ極度の熱が反応から生じます。
水素を使用するもう 1 つの活動は歯科治療です。うがい薬の代わりに
過酸化水素を
口の中に吹き込む人もいます。
過酸化水素は
細菌を減らし、感染症を除去し、歯を白くすることができます。実際、店頭で販売されている多くの美白製品には過酸化水素が含まれています。

クリーンエネルギー源としての水素
気候変動が世界中の
、生息地、環境、健康に被害を与え続けているため、研究者たちは化石燃料の排出による被害を軽減できるクリーンなエネルギー源を探し続けています。温室効果ガス排出の代替手段の 1 つは水素です。
水素燃料電池は、
自動車、バス、家庭、企業などに電力を供給できる一種のエネルギープロバイダーです。水素燃料電池は高価ですが、将来のクリーン エネルギーとなる可能性があります。
しかし、水素燃料電池はどのように機能するのでしょうか?水素燃料電池バスを例に考えてみましょう。水素燃料電池は、水素と酸素の化学反応によって生成されたエネルギーをバスの動力として使用します。ただし、バスは大気中に二酸化炭素 (CO
2
) を放出するのではなく、水を放出します。化学反応によって生成される生成物は水の形になります。
さらに、水素燃料電池エネルギーにはいくつかの利点があります。まず、水の排出は環境や大気に対して有害な影響を与えません。さらに、水素燃料電池の使用により化石燃料の必要性が減り、気候変動を遅らせることができます。さらに、気候変動に寄与する主な温室効果ガスである二酸化炭素は、水素燃料電池エネルギーの使用から生じるものではありません。
ただし、水素燃料電池の使用の欠点の 1 つは、クリーン エネルギー資源で使用される水素ガスを生成するために依然としてエネルギーが必要であることです。したがって、化石燃料を燃焼して水素燃料電池や水素ガスを生成することは気候変動に寄与することになり、その結果得られる水素燃料電池は、その製造で失われた再生不可能なエネルギーを補えない可能性があります。
水素のモル質量を発見し、他の元素とどのように比較するか イメージギャラリー











関連動画!
Molar Mass of H2O2: Hydrogen peroxide
How to Find the Mass of One Molecule of H2 (Diatomic Hydrogen)






