コンテンツ
導入
多くの人は
原子
や
分子
について聞いたことがあると思いますが、それらは何であり、それらの化学的性質は何でしょうか?定義上、原子はすべての物質の基本的な構成要素です。これにより、それは世界で最小の自然発生物になります。陽子、中性子、中性子と呼ばれる素粒子が原子を構成しています。特定の原子は、これらの亜原子粒子のそれぞれの数が異なります。
ただし、中性に帯電した原子は通常、すべて同じ数の陽子と電子を持っています。これらの原子は結合して分子を形成することができます。分子は、純粋な物質の最小単位を構成する少なくとも 2 つの原子で構成されます。これらの小さな単位は、純粋な物質の化学的特性と形成を失うことなく分裂し、結合することもできます。化学結合はこれらの分子を構成する原子を結合し、さまざまな分子構造を作成します。分子の概念は非常に単純に見えるかもしれませんが、非常に複雑な場合があります。読み続けて、極性を含む分子の化学的特性についてすべて学びましょう。
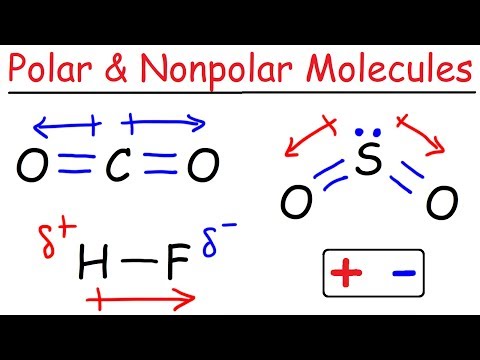
極性
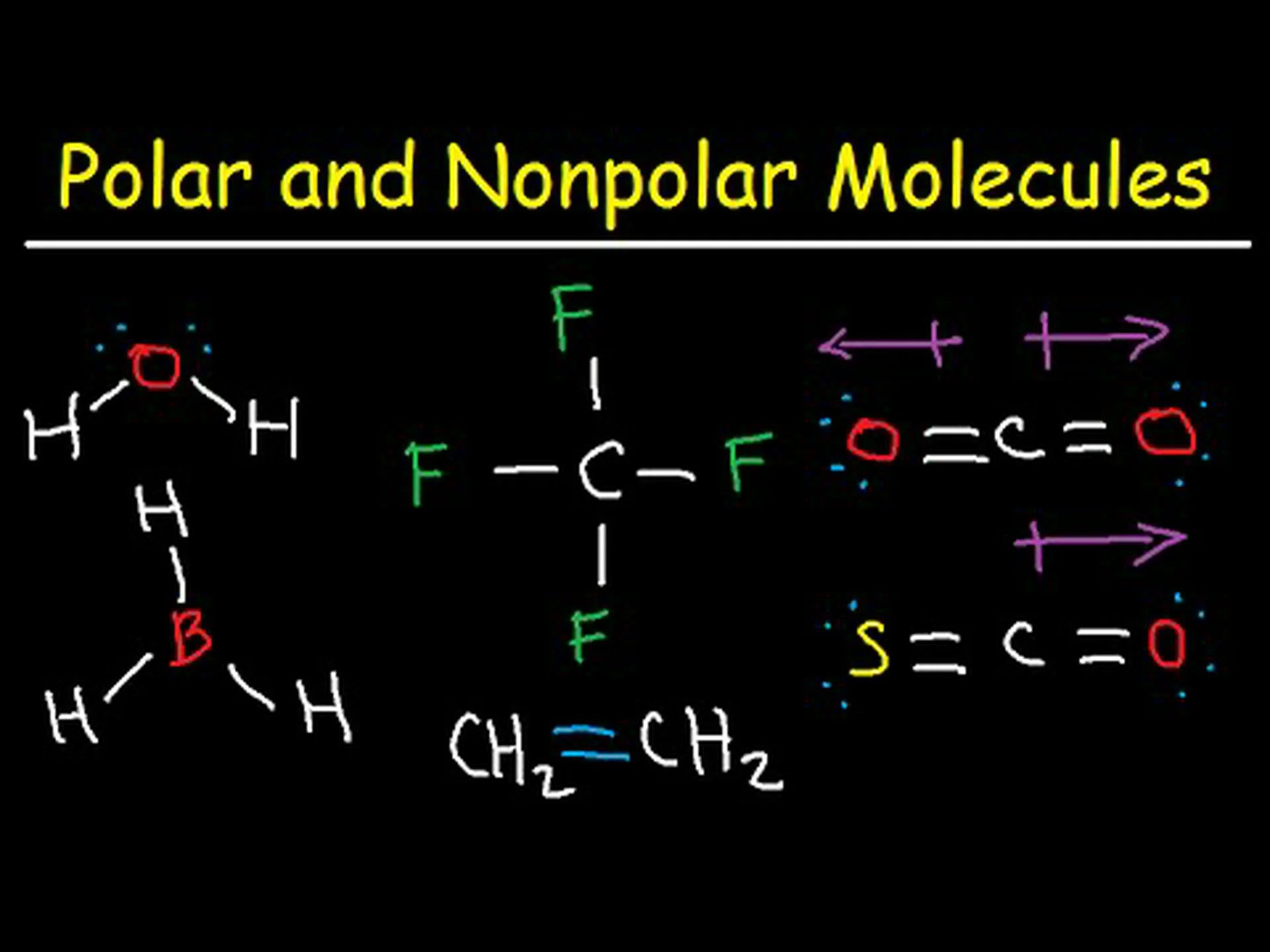
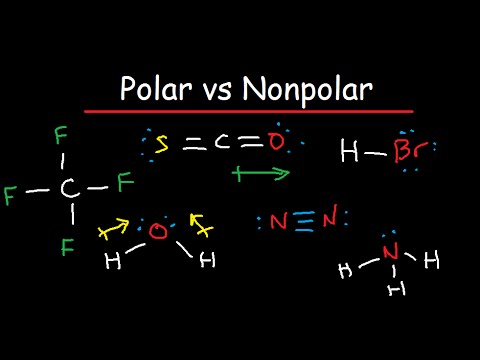
分子の主な化学的特性の 1 つは極性です。極性とは、原子間の分子の電荷の分布を指します。この分布により、分子が極性または非極性のいずれかとして識別されます。2 つの異なる分類の意味は次のとおりです。
非極性分子
電荷が分子全体に均等に分布している場合、その分子は非極性として分類できます。これらの分子は
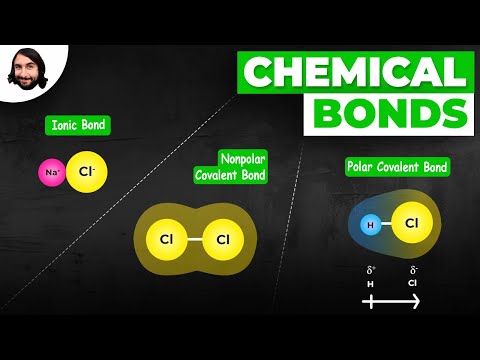
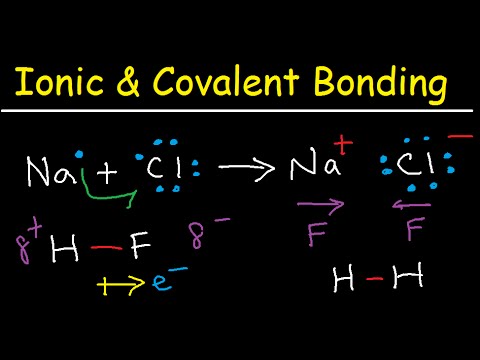
共有結合によって
分子を保持しており、原子は電子を共有することで結合します。非極性分子はその電荷により水と混合しないため、識別が容易になります。非極性分子の例には、二酸化炭素、酸素ガス、エストロゲン、コレステロールなどがあります。
極性分子
非極性分子と同様に、極性分子は共有結合によって結合されます。ただし、これらの分子は電気的分布が異なります。極性分子では、電荷は原子全体に均一に分布しません。これにより、互いに引き付けられる分子のわずかにプラスの端とわずかにマイナスの端が作成されます。極性分子の最も一般的な例は水です。酸素原子は強い電荷を持っているため、2 つの水素原子を自分自身に引き寄せます。この引力によりマイナスに帯電した領域が形成され、分子のもう一方の極はプラスに帯電したままになります。分子の極にある異なる電荷が極性の名前の由来です。他の種類の極性分子には、アンモニア、二酸化硫黄、硫化水素などがあります。

電気陰性度
分子内の異なる電荷は電気陰性度によって決まります。電気陰性度は、原子が結合するために電子を自分自身に引き寄せる強さを指します。 1932 年にライナス・ポーリングによって初めて説明されたこの概念は、2 つの原子間の共有結合の予想される強さによって決定されます。ポーリングは、分子内の異なるエネルギーに基づいてさまざまな分子の電気陰性度を決定する方程式を考案しました。その後、
周期表は
電気陰性度の観点から整理されました。表の左側には電気陰性度が最も低い分子が表示され、右側には電気陰性度が最も高い分子が表示されます。この組織は、分子とその相互作用について詳しく知りたいと考えている科学者にとって非常に役立ちます。電気陰性度の反対は電気陽性です。これは、元素がより強い電荷を持つ他の原子に
価
電子を供与する傾向を指します。

双極子モーメント
双極子モーメントは、分子内の原子間の電荷の分離を指します。この分離は、共有結合と
イオン結合の
両方によって発生する可能性があります。原子の電気陰性度に大きな違いがある場合、双極子モーメントははるかに大きくなります。電気陰性度の大きい原子は、2 つの原子間で共有されている電子を引き寄せ始め、この双極子モーメントが発生します。これらのモーメントはデバイ単位で測定され、電荷と分子内の 2 つの電荷間の距離を乗算することで求められます。最も認識可能な双極子モーメントの 1 つは、
塩化水素
分子で発生します。

化学における極性の応用
実験を行うとき、化学者は多くの場合、特定の化学物質または元素を他の物質に
溶解する
必要があります。このプロセスでは、分子の極性と化学的特性の理解が重要な役割を果たします。化学者は、極性化合物が他の極性化合物を溶解し、非極性分子も同様に溶解することを知っています。物質を溶解しようとするとき、化学者は実験をスムーズに進めるために元素の極性を認識する必要があります。これは、現代化学における極性の多くの応用例の 1 つにすぎません。
極性と非極性の分子の化学的性質の理解 イメージギャラリー








関連動画!
Polar vs Nonpolar – Amoeba Sisters #Shorts
Polar vs Nonpolar molecules: How to tell? [GCE A Level Chemistry]